Естественное течение экспериментального инфаркта миокарда
Адекватность экспериментальной информации о роли лимфатической системы сердца в развитии инфаркта миокарда в большой мере зависит от метода его воспроизведения.
Существующие модели содержат серьезные недостатки, влияющие на получаемые результаты. Естественно, что требовать от экспериментального инфаркта миокарда полного соответствия клинической картине у человека нереально. Однако без понимания и устранения принципиальных отличий можно оказаться в плену ложных представлений.
В обширной литературе, посвященной моделированию инфаркта миокарда, имеются лишь единичные работы, раскрывающие участие лимфатической системы в развитии инфаркта миокарда.
Это объяснимо: выбор модели отражает существующий уровень знаний. А он в отношении роли лимфатической системы в развитии инфаркта миокарда до последних лет был, как известно, минимальным. Поэтому потребовалось специальное рассмотрение проблемы моделирования инфаркта миокарда с интересующих нас «лимфологических» позиций.
В основе патогенеза инфаркта миокарда человека, как известно, часто лежит атеросклеротический процесс, который захватывает не только венечные артерии, но и лимфатические сосуды сердца.
В литературе рассмотрена проблема возможных отличий течения инфаркта миокарда у человека с разной степенью атеросклеротического поражения венечных артерий.
Моделирование инфаркта миокарда у животных без исходного коронарного атеросклероза и связанных с ним изменений уже содержит возможность получения неадекватной информации.
Вопрос о различиях, которые могут возникнуть при постановке эксперимента на животных с атеросклеротическими изменениями в лимфатической системе сердца и без них, в настоящее время ответа не имеет. Можно лишь чисто теоретически считать, что отличия имеются.
Сказанное в отношении атеросклеротического фона относится ко многим другим «факторам несоответствия» модели и болезни. Особого внимания, как нам кажется, требует способ, а также условия осуществления коронарной окклюзии.
Для моделирования инфаркта миокарда (ИМ) используют экстра- и интравазальные подходы к коронарным артериям.
«Инфаркт миокарда», Я.Д.Мамедов
Протромбиновый индекс по сравнению с показателем у интактных животных был достаточно повышен (более чем на 20%) во все сроки исследования. При сравнении с контролем-1 выраженных изменений не отмечалось. Таким образом, анализ полученных данных показывает, что острый инфаркт миокарда в сочетании с блокированием регионарного лимфодренажа сопровождается более резкими гиперкоагуляционными изменениями и угнетением фибринолиза в лимфе и…
Через сутки после моделирования у всех экспериментальных животных обнаруживается более обширная зона некроза, чем при одноэтапной модели. У некоторых животных зона некроза охватывает значительную поверхность передней и боковой стенки желудочка. В некротизированных мышечных клетках отсутствуют ядра, в некоторых миокардиоцитах — кариопикноз или кариолизис. В указанных участках полностью исчезает активность окислительно-восстановительных ферментов, отсутствует гликоген. Кардиомиоциты разрыхлены,…
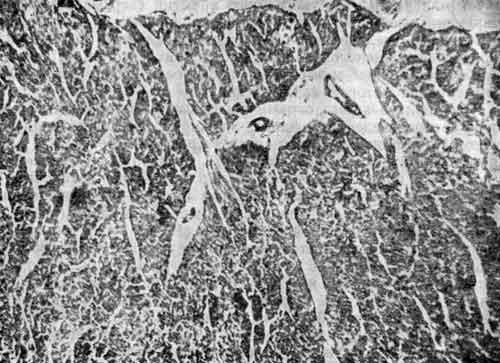
Материал для морфологического анализа брали после плановой эвтаназии или в результате гибели животного. Через 40 дней после имплантации электрода (без электротермокоагуляции) сохранена проходимость передней межжелудочковой артерии сердца. Обнаружено небольшое сужение в месте фиксации электрода, разрастание соединительной ткани вокруг электрода. При гистологическом исследовании миокарда передней стенки левого желудочка в миоцитах не обнаружена дистрофических изменений, связанных с…
Состояние передней межжелудочковой артерии (ПМЖА) сердца собак при воздействии противотромботическими препаратами № групп Группа животных Общее количество животных Состояние ПМЖА количество животных с облитерированвой ПМЖА количество животных с необлнтерированной ПМЖА 1 Животные, не получавшие прогивотромботических средств (13 собак, не получавших препаратов, и 8 собак, получавших изотонический раствор) 21 19 2 2 Животные, получавшие гепарин 8…

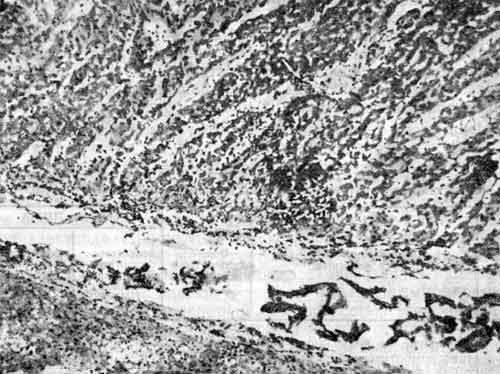
Морфологические изменения, обнаруживаемые через 7 сут, характеризуются дальнейшим развитием изменений. Область инфаркта отделяется от окружающей ткани зоной лейкоцитарной инфильтрации, фибробластами и макрофагами, обнаруживаются атрофия миоцитов вблизи эпикарда, расширение просвета сосудов, заполненных эритроцитами, в сочетании с развитием грануляционной ткани. В зоне инфаркта большая часть мышечных волокон некротизирована. Замещение пораженного участка миокарда Замещение пораженного участка миокарда грануляционной…
Выяснение роли нарушений лимфокоагуляции и лимфотромбоза: в патогенезе инфаркта миокарда потребовало моделированияпроцесса, который гарантирует выключение лимфодренажной функции сердца. С этой целью были проведены эксперименты, в которых модель инфаркта миокарда сочеталась с лигированием главного лимфатического коллектора сердца. Выживаемость Оценка результатов исследований этой серии показала, что после перевязки только коронарной артерии (контроль) пали 14 кроликов из 35,…
При параллельной перевязке коронарной артерии и лимфоколлектора сердца нарушения ЭКГпоказателей были более резкими и выявлялись в ранние сроки исследования, чем в опытах, где производилась перевязка только коронарной артерии. Так, если в контрольной серии образование комплекса QS происходило через 24 ч, то в данной серии это выявлялось уже через 3 ч после перевязки. При этом следует…
Изменения лимфокоагуляции носили следующий характер. Время свертывания на 1-е сутки после моделирования сокращалось на 72,2% (р < 0,001) по сравнению с показателем у интактных животных и на 27,1% (р < 0,01) по отношению к показателю у животных контроля (инфаркт миокарда без перевязки лимфоколлектора). На 3-и и 7-е сутки после перевязки коронарной артерии и лимфоколлектора сердца…
Показатель времени рекальцификации через сутки после моделирования снижался на 47,6% (р < 0,001) по сравнению с показателем у интактных животных и не изменялся до конца недели (ниже исходного уровня на 48,4 и 46,4%, р < 0,001). По отношению к показателю у животных контроля-1 выявлялось незначительное снижение во все сроки исследования. Толерантность к гепарину на 1-е…
Гепариновое время в 1-е и 3-и сутки острого инфаркта миокарда с блокированным лимфооттоком было меньше исходного значения на 55,9 и 59,6 % (р < 0,001) соответственно и на 7-е сутки наблюдалось увеличение на 13,7% по отношению к предшествующему сроку исследования. Сравнение с контролем на 1-е и 3-и сутки показало колебание значения гепаринового времени в пределах…
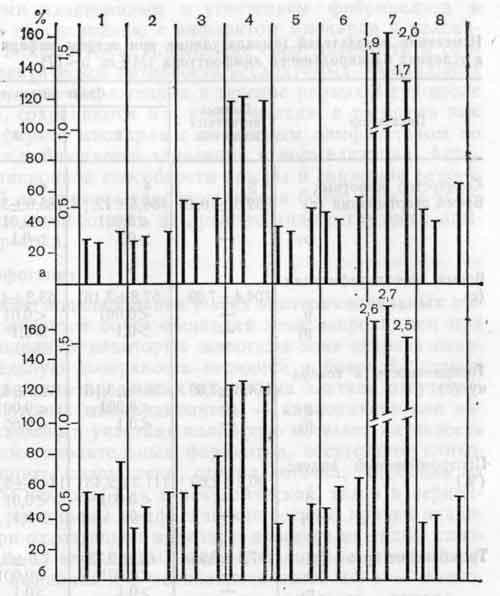
Изучение скорости лимфооттока из дренированного грудного лимфатического протока у кроликов с острым инфарктом миокарда в условиях блокирования лимфодренажа сердечной мышцы показало его выраженное уменьшение на 1-е и 3-и сутки после моделирования. В эти сроки она была меньше, чем у интактных животных. Нарастание свертывающего потенциала и угнетение фибринолиза в лимфе и крови при сочетании модели инфаркта…
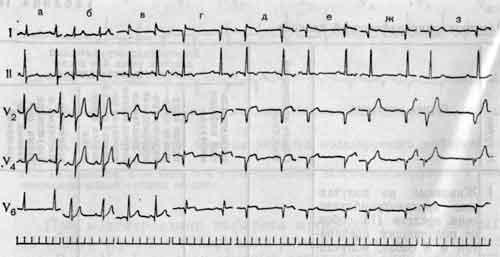
Через 3 ч у 12 из 21 собаки (57,1%) отмечены признаки очагового трансмурального инфаркта миокарда. У этих животных обнаружено исчезновение зубца R и появление комплекса QS в некоторых грудных (особенно V2-3) отведениях, смещение сегмента ST и отрицательные зубцы Т в I — II стандартных и во всех грудных остведениях, а также углубление зубцов Q в…
