Ученые открыли новый способ разработки лекарств без побочных эффектов
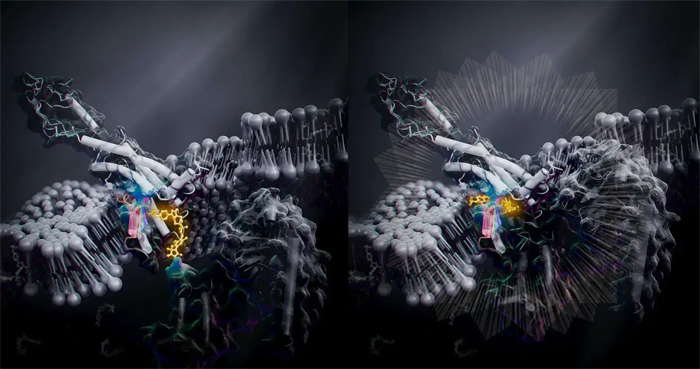
Впечатление художника от активации GPCR изнутри клетки и полученного в результате целенаправленного ответа. Авторы и права: Кобаяши и Каваками и др., 2023 г.
Ученые открыли новый способ активации рецепторов, связанных с G-белком, изнутри клеток, и это прорыв, который помогает разрабатывать лекарства без побочных эффектов.
Вы когда-нибудь задумывались, как наркотики достигают своей цели и выполняют свою функцию в нашем организме? Представьте молекулу лекарства или лиганд в качестве сообщения, а рецептор клеточной мембраны — в качестве почтового ящика. Одним из таких рецепторов, передающих молекулярные сигналы, является рецептор, связанный с G-белком (GPCR).
Активация G-белка
Интересно, что около трети всех существующих лекарств работают, контролируя активацию этого белка. Японские исследователи открыли новый способ активации GPCR, вызывая изменение формы во внутриклеточной области рецептора. Этот новый процесс может помочь исследователям разрабатывать лекарства с меньшим количеством побочных эффектов или вообще без них.
Если клеточная мембрана похожа на сэндвич с печеньем Oreo, то GPCR похожа на змею с семью сегментами, пересекающими поверхность сэндвича с печеньем и выходящими из нее. Внеклеточные петли являются почтовым ящиком для сообщений. Когда сигнальная молекула связывается с внеклеточной стороной рецептора, она запускает изменение формы, активирующее G-белки и белок β-аррестин, прикрепленный к внутриклеточной стороне рецептора. Подобно молекулярному реле, информация проходит вниз по течению и влияет на различные телесные процессы. Именно так мы видим, обоняем и ощущаем вкус, которые являются ощущениями света, обоняния и вкуса.
Неблагоприятные побочные эффекты возникают, если лекарства, действующие на GPCR, активируют несколько сигнальных путей, а не конкретный путь-мишень.
Вот почему разработка лекарств направлена на активацию специфических молекулярных сигнальных путей внутри клеток. Активация GPCR изнутри клетки, а не снаружи клетки, может быть одним из способов достижения специфичности. Но до сих пор не было доказательств прямой активации только внутриклеточной стороны GPCR без инициации с внеклеточной стороны.
Группа исследователей во главе с Осаму Нуреки, профессором Токийского университета , и его лаборатория обнаружили новый способ активации рецептора GPCR, связанного с метаболизмом кости, называемый рецептором паратиреоидного гормона человека типа 1 (PTH1R), без передачи сигнала от внеклеточной сторона.
- «Понимание молекулярного механизма позволит нам разрабатывать оптимальные лекарства», — говорит Казухиро Кобаяши, докторант и автор исследования. Такой препарат предлагает «многообещающее лечение остеопороза».
Кобаяши проводил исследования по формированию костей на животных моделях еще со школьной скамьи.
- «Лечение остеопороза, нацеленное на PTH1R, требует строгой дозировки, имеет административные ограничения, и пока нет лучших альтернатив», — говорит он. Это побудило их команду искать лучшие стратегии разработки лекарств, нацеленных на рецептор паратиреоидного гормона.
Чтобы понять функцию через структуру, они использовали криоэлектронную микроскопию и выявили трехмерную структуру белка PTH1R и G, связанного с сигнальной молекулой.

Команда синтезировала непептидную сигнальную молекулу под названием PCO371, которая связывается с внутриклеточной областью рецептора и напрямую взаимодействует с субъединицами G-белка. Другими словами, PCO371 активирует рецептор после попадания в клетку.
Как PCO371 активирует только G-белок
Структура PTH1R, связанная с PCO371, может напрямую и стабильно модулировать внутриклеточную сторону PTH1R. А поскольку PCO371 активирует только G-белок, а не ß-аррестин, он не вызывает побочных эффектов. Эта специфичность его способа связывания и активации рецептора делает его подходящим кандидатом в качестве потенциальных низкомолекулярных препаратов для GPCR класса B1, таких как PTH1R, у которых в настоящее время отсутствуют лиганды для перорального введения. Такие лекарства могли бы уменьшить побочные эффекты и нагрузку на пациентов, поскольку они действуют на определенные молекулярные пути.
Результаты этого исследования помогут «разработать новые лекарства от таких заболеваний, как ожирение, боль, остеопороз и неврологические расстройства».
Метки: Белок

Исследователи из Института науки Вейцмана в Израиле выявили дрожжи, которые можно использовать для предотвращения инвазивного кандидоза, основной причины смерти госпитализированных пациентов и пациентов с ослабленным иммунитетом. Исследование, недавно опубликованное в Журнале экспериментальной медицины (JEM), показывает, что новые дрожжи безвредно живут в кишечнике мышей и людей и могут вытеснять дрожжи, ответственные за кандидоз, Candida albicans. Микробы…
Недавние исследования выявили решающую роль метилирования ДНК в черепно-лицевом развитии, открывая путь к предотвращению расщелины губы и неба путем понимания воздействия окружающей среды на генетическую экспрессию. Расщелина губы и неба — наиболее распространенные черепно-лицевые врожденные дефекты у человека, ежегодно поражающие более 175 000 новорожденных во всем мире. Тем не менее, несмотря на десятилетия исследований, до…
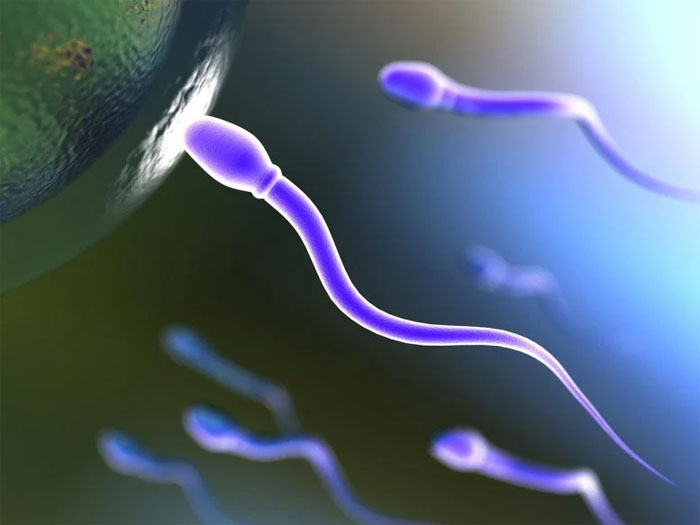
Исследователи из Университета штата Мичиган разгадали загадку менее изученной структуры сперматозоида, известной как цитоплазматическая капля (ЦК). CD, характеризующийся увеличенной цитоплазмой — вязким желеобразным веществом, инкапсулированным клеточной мембраной, — расположен рядом с головкой сперматозоида, особенно на его шейке. Это явление наблюдается у всех млекопитающих, включая человека. Эта новая генетическая модель является первой в своем роде. Как…
Исследование показывает, что блокирование белка PD-L2 в стареющих раковых клетках после химиотерапии повышает способность иммунной системы разрушать эти клетки, потенциально повышая эффективность химиотерапии против рака. Лечение рака, включая химиотерапию, помимо уничтожения большого количества опухолевых клеток, также приводит к образованию стареющих опухолевых клеток (также называемых «клетками зомби»). Хотя стареющие клетки не размножаются, они, к сожалению, создают…

Переход от продуктов животного происхождения к продуктам растительного происхождения, независимо от того, считаются ли эти продукты растительного происхождения здоровыми или вредными согласно индексу растительной диеты, приводит к снижению веса у людей с избыточным весом, снижает потребление холестерина и жиров, а также увеличивает потребление клетчатки. Согласно новому анализу Комитета врачей за ответственную медицину, опубликованному в Европейском…
