Удаление алкильного радикала из первого положения имидазольного кольца
При удалении алкильного радикала из первого положения имидазольного кольца, т. е. при переходе к норантифеину и этефилу, наблюдается выраженная дифференцировка биологического действия препаратов. В частности, эти вещества утрачивают метаболические эффекты, приобретают иной характер действия на высшую нервную деятельность, но сохраняют стимулирующее влияние на функцию дыхания. В то же время электронно-конформационные характеристики этих соединений изменяются незначительно.
 Следовательно, для проявления метаболических эффектов необходим алкильный заместитель в
Следовательно, для проявления метаболических эффектов необходим алкильный заместитель в  первом положении имидазольного кольца, который обеспечивает взаимодействие с активными центрами макромолекул. Для сохранения центрального действия этих препаратов необходимо сохранить общую гидрофобность их молекулы. Гидрофильный характер незамещенного имидазольного кольца норантифеина и этефила может быть компенсирован за счет увеличения гидрофобных свойств в амидной части молекулы, что мы и наблюдаем при переходе от норантифеина к более высокоактивному этефилу.
первом положении имидазольного кольца, который обеспечивает взаимодействие с активными центрами макромолекул. Для сохранения центрального действия этих препаратов необходимо сохранить общую гидрофобность их молекулы. Гидрофильный характер незамещенного имидазольного кольца норантифеина и этефила может быть компенсирован за счет увеличения гидрофобных свойств в амидной части молекулы, что мы и наблюдаем при переходе от норантифеина к более высокоактивному этефилу.
Аналогичное явление наблюдается, повидимому, и в случае чтиразола. Гидрофобный радикал у его молекулы выведен из ближайшего положения от одной из карбоксамидных групп и перемещен по циклу в дальнее положение, эквивалентное С-2 у этимизола.
Следовательно, нарушается взаимодействие гидрофобного активного радикала с активными центрами макромолекул. Последним, вероятно, и можно объяснить исчезновение у этиразола метаболических эффектов.
Распределение электронной плотности на атоме азота «пиримидинового» типа (N-2) у этиразола резко снижено по сравнению с этимизолом.э
В определенной степени это может явиться причиной ослабления центрального действия этиразола, в том числе и на функцию памяти. Однако в большей степени это можно объяснить и стерическим препятствием со стороны этильной группы при атоме азота в первом положении пиразольного кольца в момент взаимодействия его с активными центрами макромолекул.
Последнему, повидимому, следует отдать предпочтение, так как подтверждением служат результаты изучения двух замещенных антифеинов [Бородкин Ю. С, 1960; Виноградова Н. Б. и др., 1961]. Так, введение метильного заместителя во второе положение молекулы антифсина приводит к резкому ослаблению биологической активности вещества, в то время как коэффициент распределения хлороформ — вода для этого соединения мало отличается от коэффициента распределения для самого антифеина [Кожевников С. П. и др., 1965].
Таким образом, снижение активности двух замещенных антифеинов можно объяснить в основном возникновением препятствия со стороны заместителя во втором положении имидазольного кольца к образованию комплекса с макромолекулами. Этиразол имеет этильную группу в положении, эквивалентном углероду во втором положении имидазольного кольца антифеина и этимизола.
Следовательно, и ослабление действия этиразола можно связать с теми же стерическими препятствиями к образованию комплекса, что и у двух замещенных антифеинов [Бородкин Ю. С, 1966].
«Нейрохимические и функциональные основы долговременной памяти»,
Ю.С. Бродкин, Ю.В. Зайцев
Установлено, что при повторном тестировании выработанной реакции активного избегания через сутки после окончания обучения число сочетаний, необходимое для осуществления 3 последовательных правильных ответов в контрольной группе подопытных животных, значительно уменьшается. Этот эффект практически отсутствует при тестировании ее спустя 7 сут (выработанный навык полностью утрачен). Введение в этом случае самого аденина увеличивает на 66 % число…
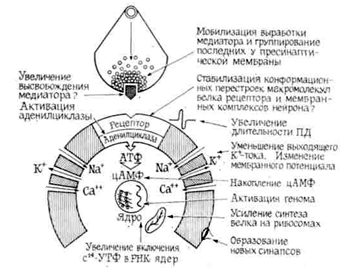
В настоящее время сложилось представление, что активация генетического аппарата нервных клеток является пусковым фактором в индукции синтеза макромолекул (РНК, полипептиды), которые принимают участие в процессах обучения и памяти. Одним из важнейших показателей активности генетического аппарата клеток является РНК-полимеразная активность ядер, характеризующая уровень транскрипции хроматина. Поэтому было изучено влияние этимизола на синтез РНК в изолированных ядрах…

Для этиразола также свойственны четыре конформационные формы, причем при переходе из конформации А, которая является наиболее предпочтительной, в конформацию В требуется не 38,4 кДж/моль, как у этимизола, а всего 12,95 кДж/моль. В то же время переход из конформации А в конформацию Б, как и в первом случае, требует всего 1,6 — 1,7 ккал/моль. Следовательно, этиразол…
Этимизол повышал уровень кортикостероидов в плазме крови наиболее эффективно спустя 40 мин после его введения. Эта же тенденция, но, естественно, в меньшей мере, сохранялась и после двусторонней адреналэктомии. Уровень содержания кортикостероидов (мкг) в плазме крови после введения этимизола Группы животных Уровень кортикостероидов через 20 мин через 40 мин Неоперированные: контроль (20) 17,8±2,1 — этимизол (20)…

Методом теоретического конформационного анализа, а также ЯМР- и ИК-спектроскопии было показано, что молекулы этимизола и его производных имеют значительные конформационные ограничения; из всех возможных конформации реализуется главным образом одна, стабилизированная прочной внутримолекулярной водородной связью и имеющая, таким образом, сравнительно жесткую бициклическую структуру. Внутримолекулярная водородная связь образуется между двумя карбоксамидными группами. Конформационная стабилизация последних способствует образованию…
